الجدول الدوري الحديث.. من هو الذي اخترع الجدول الدوري الحديث؟
كانت للكيمياء أثر كبير في حياتنا، بها عرفنا أن نقوم بعمل المركبات العلاجية وغيرها من المركبات التي ساعدتنا على التطور في حياتنا على مر العصور والوقت، لذا سنتناول في موضوع هذا اليوم عن الجدول الدوري الحديث دعونا نتعرف عليه.
الجدول الدوري الحديث
دعنا نتعرف على الجدول الدوري الحديث وعلى ماذا يحتوي هذا الجدول هيا لنتعرف عليه:
- يضم الجدول الدوري جدول العناصر المعروفة بالنسبة للإنسان وفقاً للعدد الذري المتزايد والخصائص الكيميائية المتكررة.
- يتمثل كل عنصر في رمزه الكيميائي مثل cu .
- الجدول الدوري الحديث يحتوي على 7 دورات أفقية و 18 مجموعة رأسية.
دورات الجدول الدوري الحديث
يوجد نوعين من الدورات في الجدول الدوري لذا دعنا نتعرف على كلاهما:
1– الدورات الأفقية
تبدأ صفوف الدورة الأفقية من اليسار إلى اليمين، ويحتوي كل عنصر على بروتين واحد أقل من العنصر الذي يليه. وبالتالي يكون هناك زيادة في العدد الذري للعنصر عند الانتقال من اليسار إلى اليمين.
العناصر الموجودة على اليسار هي الفلزات، بينما اللافلزات تكون على الجانب الأيمن من الدورة.
نلاحظ وجود دورات في الجدول الدوري أطول من غيرها مثل احتواء الدورة 1 على عنصرين فقط، علي نقيض ذلك فإن الدورتين 6 و 7 طويلة بحيث يكون هناك اتاحه في وضع العديد من عناصرها أسفل الجدول .
2- الدورات الرأسية
تعد العناصر في نفس المجموعة لها نفس الخصائص مثل جميع العناصر داخل المجموعة 18 وهي غازات خاملة لا تحتوي على أي رائحة أو لون.
يتم الترقيم من 1 الفلزات القلوية إلى الغازات النبيلة وتشترك العناصر مع مجموعة لتكوين إلكترون التكافؤ.
يحدث تزايد في نصف القطر الذري عند التحرك من أعلى إلى أسفل المجموعة وتكتسب العناصر التي تلى بعضها مستوى طاقة جديدة.
عند التحرك من أعلى إلى أسفل فأن السالبية الكهربية تقل، وذلك بسبب إضافة غلاف إلكتروني يدفع إلكترونات التكافؤ بعيداً عن النواة، و تصبح للعناصر طاقات تأين أفل على التوالي لأنه يصبح من السهل إزالة إلكترون.
مخترع الجدول الدوري الحديث
قام العالم الكيميائي الروسي ديمتري مندلييف بوضع أول جدول دوري كيميائي بشكل متزامن تقريبا مع جدول ثاني كان بأنشائه الألماني لوثر ماير وبسبب ذلك حصل كلامها على ميدالية ديفي التي تسندها الجمعية الملكية البريطانية.
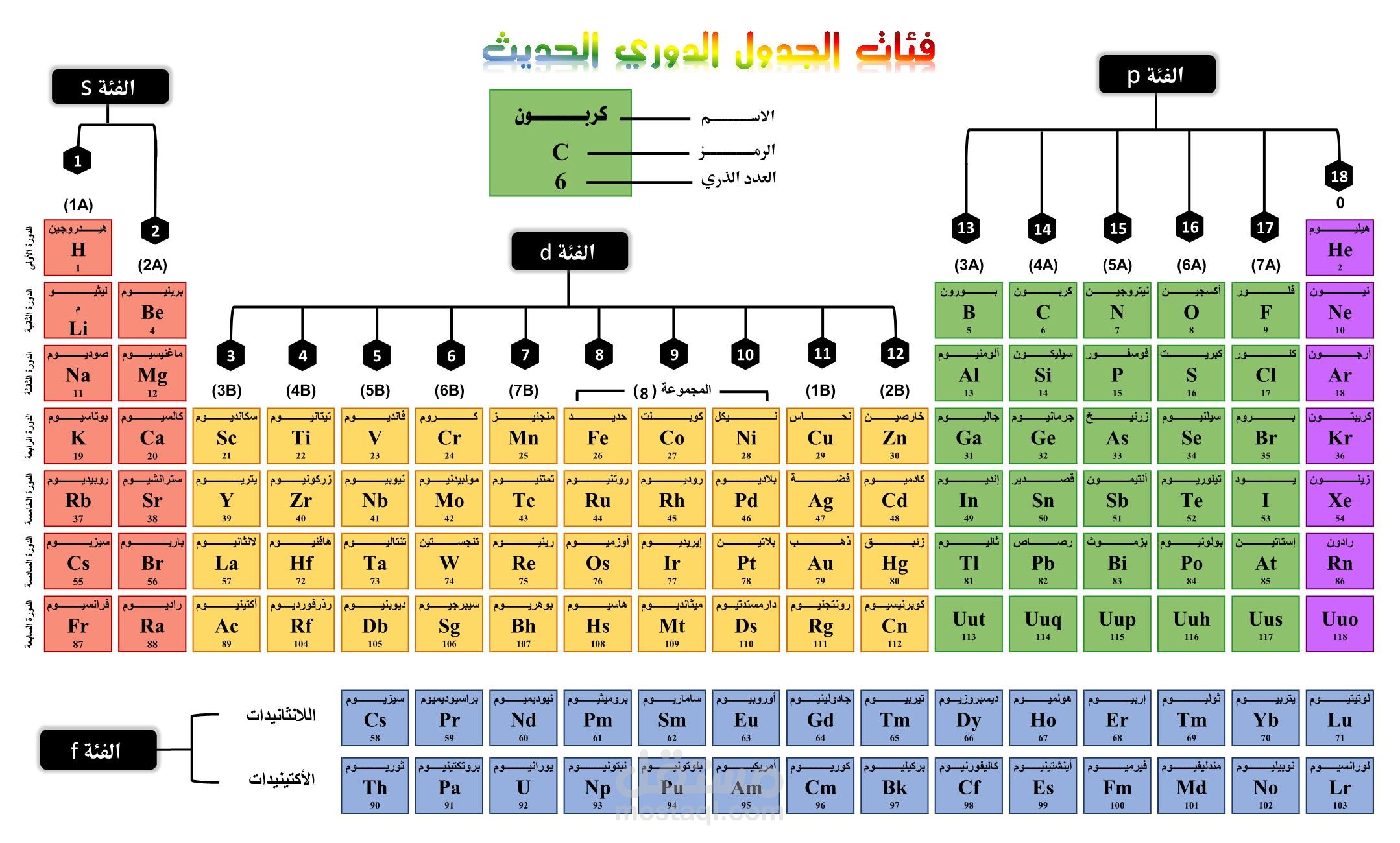
فئات الجدول الدوري الحديث
تنقسم فئات الجدول الدوري الحديث إلى أربعة فئات هيا لنتعرف عليها واحداً تلو الأخر:
- الفئة s التي تشمل أول مجموعتين من الأتربة القلوية والفلزات القلوية والهيدروجين والهيليوم.
- الفئة p وتشمل المجموعات من 13 إلى 18.
- الفئة d و تشمل المجموعات من 3 إلى 12 وهي تعتبر المعاد الانتقالية.
- الفئة f وتتكون من فترتين أسفل الجدول الدوري الرئيسي (اللانثانيدات والأكتنيدات).
عناصر مجموعات الجدول الدوري
إليك بعض من عناصر مجموعات الدوري الحديث هيا لنتعرف عليها عنصر تلو الأخر:
| المجموعة الأولى | المجموعة الثانية | المجموعة الثالثة | المجموعة الرابعة | المجموعة الخامسة | المجموعة السادسة | المجموعة السابعة | المجموعة الثامنة |
| الهيدروجين | البيريليوم | البورون | الكربون | النيتروجين | الأكسجين | الفلور | الهيليوم |
| الليثيوم | المغنيسيوم | الألومنيوم | السيليكون | الفسفور | الكبريت | الكلور | النيون |
| الصوديوم | الكالسيوم | الغاليوم | الجيرمانيوم | الزرنيخ | السيلينيوم | البروم | الأرجون |
| البوتاسيوم | السترونتيوم | الإنديوم | القصدير | الأنتيمون | التيلوريوم | اليود | الكريبتون |
| السيزيوم | الباريوم | الثاليوم | الرصاص | البزموث | البولونيوم | الأستاتين | الزينون |
| الفرانسيوم | الراديوم | النيهونيوم | فليروفيوم | المسكوفيوم | الليفر مريوم | التينيسين | الرادون |
على الرغم من اكتشاف أو تصنيع عناصر الجدول الحديث إلا أنها تحتوي على حياة المليارات من البشر، تلك العناصر التي تدخل في تصنيع أساسيات الحياة كالأدوية وغيرها من الأشياء التي نستخدمها بشكل يومي.
Questions & Answers
مخترع الجدول الدوري الحديث هو العالم الكيميائي الروسي ديمتري مندلييف.
الدورات التي يتكون منها الجدول الدوري الحديث، الدورات الرأسية والدورات الأفقية.
تنقسم الجدول الدوري الحديث إلى أربعة فئات.


تعليقات